Come la temperatura influenza il valore del pH
20 feb 2023
Prodotto
Anche piccoli cambiamenti di temperatura possono avere un impatto significativo sulle misurazioni del pH, poiché i due sono collegati. La temperatura influenza una misurazione del pH in diversi modi. Questo articolo del blog discuterà su come gestire i diversi effetti della temperatura sulle misurazioni del pH.
Clicca per andare direttamente all'argomento:
- Perché la temperatura influisce sul valore del pH?
- Effetti della temperatura sulla misurazione del pH e come gestirli
– Scelta di una membrana di vetro appropriata
– Corretto posizionamento del sensore di temperatura e dell'elettrodo pH
– Elettrodi pH combinati con sistema di riferimento «Long Life»
Perché la temperatura influisce sul valore del pH?
La temperatura e il valore del pH sono correlati dall'equazione di Nernst. Questa equazione descrive la relazione ideale tra l'attività aM di uno ione di misura in soluzione e il potenziale misurato tra l'elettrodo di riferimento e l'elettrodo di misura. La temperatura influenza il potenziale di Nernst, comunemente chiamato pendenza nella misurazione del pH.

Da questo, la pendenza UN può essere calcolata:
Una variazione di temperatura di 1 °C corrisponde a una variazione di 0,2 mV. Per dirla in termini relativi: una differenza di pH di 0,01 corrisponde a 0,6 mV. Pertanto, è necessario tenere conto della temperatura in tutte le misurazioni del pH. In caso contrario, non si otterranno risultati corretti se non si conoscono le temperature di calibrazione e misurazione.
La pendenza UN è diversa per diverse temperature. A T = 298,16 K = 25 °C e z = 1, la pendenza UN è pari a 59,16 mV. Per altre temperature, nell'equazione di Nernst viene utilizzato un valore diverso per la pendenza UN. Questo si chiama compensazione della temperatura. La Tabella 1 elenca il valore della pendenza per diverse temperature.
Tabella 1. Dipendenza dalla temperatura della pendenza.
| Temperatura T [°C] | Pendenza UN [mV/pH unit] |
Temperatura T [°C] | Pendenza UN [mV/pH unit] |
|---|---|---|---|
| 0 | 54.20 | 50 | 64.12 |
| 5 | 55.19 | 55 | 65.11 |
| 10 | 56.18 | 60 | 66.10 |
| 15 | 57.17 | 65 | 67.09 |
| 20 | 58.16 | 70 | 68.08 |
| 25 | 59.16 | 75 | 69.07 |
| 30 | 60.15 | 80 | 70.07 |
| 35 | 61.14 | 85 | 71.06 |
| 37 | 61.54 | 90 | 72.05 |
| 40 | 62.13 | 95 | 73.04 |
| 45 | 63.12 | 100 | 74.03 |
I moderni misuratori di pH includono una funzione per la compensazione della temperatura. Ciò significa che non appena un sensore di temperatura viene collegato al pHmetro, la dipendenza dalla temperatura della pendenza UN viene automaticamente considerata e corretta. La misurazione della temperatura non solo aiuta a garantire misurazioni accurate del pH, ma garantisce anche la conformità alle linee guida GLP/ISO che richiedono la registrazione della temperatura per tutte le misurazioni.
Effetti della temperatura sulla misurazione del pH e come gestirli
Il valore del pH è probabilmente il parametro più comunemente misurato in chimica analitica. Influenza, tra le altre cose, le caratteristiche del prodotto, le reazioni chimiche e biochimiche e i processi fisiologici. Spesso sono necessarie condizioni ambientali costanti per ottenere risultati di misurazione precisi.
In alcuni casi le variazioni di temperatura non possono essere evitate. Ad esempio, la semplice apertura di una porta può provocare un cambiamento della temperatura ambiente. Anche lavorando in ambienti climatizzati possono verificarsi reazioni esotermiche con conseguente aumento della temperatura. Le cause delle fluttuazioni di temperatura non potrebbero essere più varie, quindi questa sezione ti darà alcuni suggerimenti per la preparazione. Seguirli per ridurre al minimo o addirittura eliminare i possibili effetti legati alla temperatura prima di iniziare la calibrazione/misurazione del pH.
Scelta di una membrana di vetro appropriata
Per coprire le misurazioni del pH in un'ampia gamma di campioni, Metrohm offre elettrodi pH con diversi tipi di membrana in vetro.

A temperature più elevate l'elettrodo pH invecchia più velocemente, il che porta ad un aumento della resistenza della membrana. Pertanto, diventa più difficile per gli ioni idronio passare attraverso la membrana. Ciò può modificare il potenziale di equilibrio dell'elettrodo, causando uno spostamento nella lettura del pH.
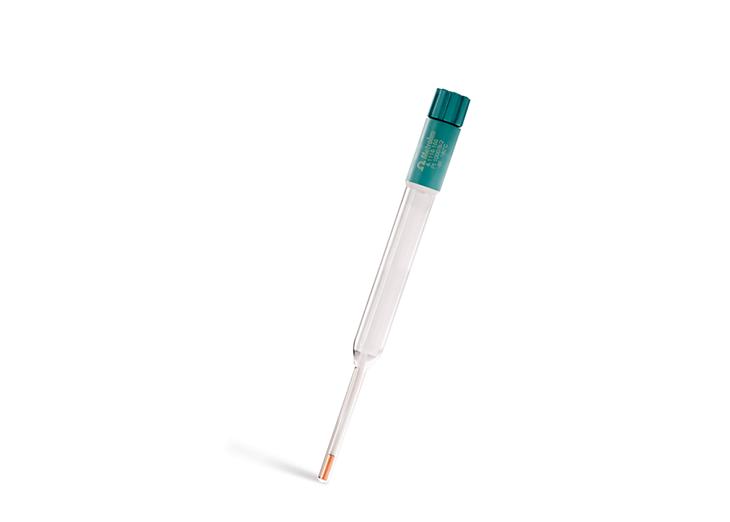
Per misure di pH a temperature più elevate, utilizza un elettrodo pH con membrana in vetro «U» di colore verde in quanto sono più resistenti al calore.
- Esempio: Metrohm Unitrode (Figura 1)

Le misurazioni del pH a basse temperature mostrano effetti simili. A temperature più basse, la membrana diventa più rigida e anche il trasporto di ioni è più difficile. Inoltre, l'attività degli ioni idrogeno nella soluzione elettrolitica diminuisce a basse temperature. Entrambi gli effetti si traducono in un aumento della resistenza della membrana.
In parole povere, quando la soluzione di misura viene raffreddata di 10 K, la resistenza della membrana raddoppia [1,2].
Per misure di pH a temperature più basse, si consiglia un elettrodo con una membrana di vetro a «T» di colore blu e un elettrolita di riferimento addensato poiché l'elettrolita di riferimento contiene solventi che agiscono da antigelo.
- Esempio: Metrohm Porotrode (Figura 2)
Corretto posizionamento del sensore di temperatura e dell'elettrodo pH
Assicurati che il sensore di temperatura sia posizionato nelle immediate vicinanze della membrana di vetro dell'elettrodo pH. In caso contrario, la temperatura della soluzione di misurazione non può essere misurata correttamente.
Inoltre, la compensazione del pH non sarà corretta in quanto la temperatura e il pH non vengono misurati nello stesso punto.
Per evitare completamente questo effetto, utilizza un elettrodo pH con sensore di temperatura integrato. In questo caso, il sensore di temperatura si trova all'interno dell'elettrodo nelle immediate vicinanze della membrana di vetro (Figura 3).


Elettrodi pH combinati con sistema di riferimento «Long Life».
La maggior parte degli elettrodi per pH disponibili sul mercato sono elettrodi per pH combinati con il sistema di riferimento Ag/AgCl. Il prodotto di solubilità del cloruro d'argento dipende dalla temperatura.
Il prodotto di solubilità del cloruro d'argento in acqua è molto piccolo a circa 10-10 mol2/L2. Tuttavia, il cloruro d'argento si dissolve molto facilmente in caso di formazione di complessi. L'aumento della temperatura favorisce questo effetto, determinando un cambiamento dell'equilibrio tra cloruro d'argento solido e disciolto. Pertanto, se la temperatura cambia, è necessario attendere che venga nuovamente raggiunto un equilibrio stabile, in quanto questo equilibrio determina il potenziale dell'elettrodo di riferimento.
Grazie al sistema di riferimento «Long Life» utilizzato negli elettrodi pH Metrohm (Figura 4), l'equilibrio termodinamico tra argento, cloruro d'argento (solido) e cloruro d'argento (disciolto) viene stabilito molto rapidamente e il potenziale dell'elettrodo di riferimento diventa stabile dopo pochissimo tempo.

Calibrazione dell'elettrodo pH
Gli elettrodi pH Metrohm sono costruiti secondo DIN 19263. Gli elettrodi pH Metrohm sono costruiti secondo DIN 19263. Questi elettrodi presentano una lettura potenziale di 0 mV (punto zero) intorno a pH 7. Come precedentemente spiegato, secondo l'equazione di Nernst, la pendenza dell'elettrodo e (in determinate circostanze) anche il punto zero dell'elettrodo cambiano quando l'elettrodo pH è esposto a un cambiamento di temperatura
Considerando le curve di calibrazione (isoterme) degli elettrodi pH a diverse temperature in condizioni ideali, ci si aspetterebbe che si intersechino nel punto zero dell'elettrodo. Sfortunatamente, questo non è il caso degli elettrodi pH nella vita reale. Si forma un punto di intersezione isotermico (Figura 5) vicino al punto zero dell'elettrodo. Quanto vicino dipende dalle condizioni dell'elettrodo.
Per ridurre al minimo tali effetti, la calibrazione dell'elettrodo pH deve essere effettuata alla stessa temperatura che verrà utilizzata per le successive misurazioni del pH.
Temperatura delle soluzioni di misura
Il valore pH dell'acqua pura a 25 °C è 7,00. In questo caso, nell'acqua sono presenti un numero uguale di ioni idronio e idrossido. A causa della dipendenza dalla temperatura del prodotto ionico dell'acqua, questo equilibrio si sposta verso un pH più alto a temperature più basse e viceversa. Questi spostamenti di equilibrio sono noti per soluzioni tampone e per acidi e basi ben noti (vedi la Tabella 2 per esempi), ma non per tutti i tipi di soluzioni campione.
Tabella 2. Tre esempi che mostrano come i cambiamenti di temperatura possono influenzare il valore di pH del campione [3].
| pH di soluzioni misurate a diverse temperature | 0 °C | 25 °C | 50 °C |
|---|---|---|---|
| H2O | 7.47 | 7.00 | 6.63 |
| c = 0.001 mol/L HCl * | 3.00 | 3.00 | 3.00 |
| c = 0.001 mol/L NaOH | 11.94 | 11.00 | 10.26 |
* Gli effetti della temperatura sono più deboli per quanto riguarda la determinazione del pH delle sostanze acide. In questi casi c'è una tendenza generale all'aumento del valore del pH con l'aumento della temperatura.
Anche i più moderni misuratori di pH possono solo correggere l'andamento della temperatura dell'elettrodo, ma mai quello delle soluzioni da misurare. Per una corretta misurazione del pH, è essenziale misurare sempre il valore del pH dei campioni alla temperatura alla quale sono stati campionati. Ad esempio, se un campione viene prelevato a 10 °C, anche la calibrazione dell'elettrodo pH e la misurazione del campione devono essere eseguite a 10 °C. Seguendo questo protocollo si evitano effetti di equilibrio termico indesiderati e si ottiene una risposta più rapida dell'elettrodo pH.
Conclusione
Grazie alla loro costruzione ottimizzata, il comportamento reale degli elettrodi pH Metrohm di alta qualità si discosta solo leggermente (potenziali di asimmetria di massimo +/- 15 mV) dai valori ideali. Tuttavia, come la maggior parte delle cose, è in gioco più di un fattore.
La checklist riportato di seguito può aiutarti a ottenere risultati di misurazione precisi durante la calibrazione e la misurazione del pH. Se puoi rispondere a tutti i punti elencati con un SÌ, vengono presi in considerazione la maggior parte degli effetti causati dai cambiamenti di temperatura.
| SI / NO | |
|---|---|
| ( ) | Ho scelto un elettrodo di vetro per pH appropriato considerando il suo tipo di vetro a membrana per la mia applicazione. |
| ( ) | Il mio elettrodo pH combinato in vetro è dotato di un sistema di riferimento «Long Life». |
| ( ) | Il mio sensore di temperatura è posizionato vicino alla membrana di vetro del mio elettrodo pH. O Sto usando un elettrodo di vetro pH combinato con sensore di temperatura integrato per la mia calibrazione / misurazione del pH. |
| ( ) | Il mio pHmetro ha una compensazione della temperatura integrata. |
| ( ) | La mia calibrazione viene eseguita alla stessa temperatura di tutte le successive misurazioni del pH. |
| ( ) | Tutte le soluzioni campione da misurare sono alla stessa temperatura. |
Riferimenti
[1] Degner, R.; Leibl, S. PH Messen: So Wird’s Gemacht!; Wiley, 1995.
[2] Galster, H. PH-Messung: Grundlagen, Methoden, Anwendungen, Geräte; VCH, 1990.
[3] pH und Temperatur – zwei untrennbare Größen. Wiley Analytical Science. https://analyticalscience.wiley.com/do/10.1002/was.00050234 (accessed 2023-02-09).
La tua conoscenza "take-aways"
Monografia: Misurazione del pH dalla A alla Z
Flyer: Elettrodi per misure di pH - Quale elettrodo per quale applicazione?
Application Bulletin: Tecnica di misurazione del pH
Blog: FAQ: Tutto sulla calibrazione del pH
 Condividi l'articolo
Condividi l'articolo