Как температура влияет на значение pH
20 февр. 2023 г.
Статья
Даже небольшие изменения температуры могут существенно повлиять на измерения pH, поскольку они взаимосвязаны. Температура влияет на измерение pH несколькими способами. В этой статье в блоге будут рассмотрены причины, почему и как вы можете справиться с различными эффектами от температуры на измерения pH.
Нажмите по ссылке, чтобы перейти сразу к теме:
– Выбор подходящей стеклянной мембраны
– Правильное расположение датчика температуры и pH-электрода
– Комбинированные pH-электроды с системой сравнения «Long Life»
Почему температура влияет на значение pH?
Температура и значение pH связаны уравнением Нернста. Это уравнение описывает идеальное соотношение между активностью aM измерительного иона в растворе и потенциалом, измеренным между электродом сравнения и измерительным электродом. Температура влияет на потенциал Нернста, который чаще называют наклоном при измерении pH.
Изменение температуры на 1 °C соответствует изменению на 0,2 мВ. Говоря в относительных терминах: разница pH 0,01 соответствует 0,6 мВ. Поэтому необходимо учитывать температуру при всех измерениях pH. В противном случае вы не получите правильных результатов, если неизвестны температуры калибровки и измерения.
Наклон UN различен для разных температур. При T = 298,16 K = 25 °C и z = 1 наклон UN равен 59,16 мВ. Для других температур в уравнении Нернста используется другое значение UN. Это называется температурной коррекцией. В Таблице 1 приведены значения наклона для различных температур.
Таблица 1. Температурная зависимость наклона.
| Temperature T [°C] | Slope UN [mV/pH unit] |
Temperature T [°C] | Slope UN [mV/pH unit] |
|---|---|---|---|
| 0 | 54.20 | 50 | 64.12 |
| 5 | 55.19 | 55 | 65.11 |
| 10 | 56.18 | 60 | 66.10 |
| 15 | 57.17 | 65 | 67.09 |
| 20 | 58.16 | 70 | 68.08 |
| 25 | 59.16 | 75 | 69.07 |
| 30 | 60.15 | 80 | 70.07 |
| 35 | 61.14 | 85 | 71.06 |
| 37 | 61.54 | 90 | 72.05 |
| 40 | 62.13 | 95 | 73.04 |
| 45 | 63.12 | 100 | 74.03 |
Современные рН-метры включают функцию температурной коррекции. Это означает, что как только к рН-метру подключается датчик температуры, температурная зависимость UN автоматически учитывается и корректируется. Измерение температуры не только помогает с точностью измерения pH, но и обеспечивает соответствие рекомендациям GLP/ISO, которые требуют регистрации температуры для всех измерений.
Влияние температуры на измерение pH и как с этим работать
Значение рН, вероятно, является самым часто измеряемым параметром в аналитической химии. Оно влияет на характеристики продукта, химические и биохимические реакции и физиологические процессы. Часто для получения точных результатов измерения необходимы постоянные условия окружающей среды.
В некоторых случаях изменения температуры не избежать. Например, простое открытие двери может вызвать это изменение. Даже при работе в среде с кондиционированием воздуха могут происходить экзотермические реакции, приводящие к повышению температуры. Причины колебаний температуры очень разнообразны, поэтому в этом разделе мы дадим несколько советов. Следуйте им, чтобы свести к минимуму или даже исключить возможные температурные эффекты, прежде чем приступать к калибровке/измерению pH.
Выбор подходящей стеклянной мембраны
Для проведения измерений pH в широком диапазоне образцов Metrohm предлагает pH-электроды с различными типами стеклянной мембраны.
При более высоких температурах pH-электрод стареет быстрее, что приводит к увеличению сопротивления мембраны. Ионам гидроксония становится труднее проходить через мембрану, и это может изменить равновесный потенциал электрода, вызывая сдвиг показаний pH.
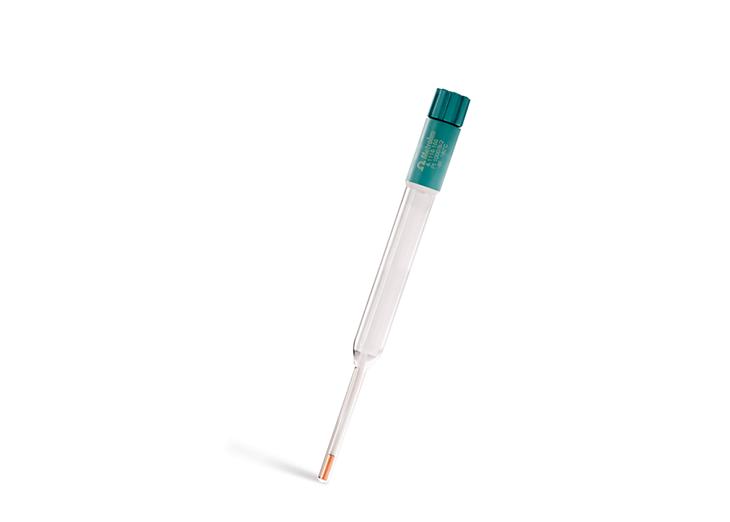
Для измерения pH при более высоких температурах используйте pH-электрод с мембраной зеленого цвета «U», поскольку они более термоустойчивы.
- Пример: Metrohm Unitrode (Рисунок 1)
Измерения pH при низких температурах показывают аналогичные эффекты. Мембрана становится более жесткой, а перенос ионов затрудняется. Кроме того, активность ионов водорода в растворе электролита снижается при низких температурах. Оба эффекта приводят к увеличению сопротивления мембраны.
Грубо говоря, при охлаждении измерительного раствора на 10 К сопротивление мембраны удваивается [1,2].
Для измерения рН в таких условиях рекомендуется использовать электрод с мембранным стеклом синего цвета «Т» и особый электролит сравнения, так как он содержит растворители, действующие как антифриз.
- Пример: Metrohm Porotrode (Рисунок 2)
Правильное расположение температурного датчика и pH-электрода
Убедитесь, что температурный сенсор расположен в непосредственной близости от стеклянной мембраны рН-электрода. В противном случае температура раствора будет измерена неправильно.
Кроме того, температурная коррекция pH будет неправильной, поскольку температура и pH не измеряются в одном и том же месте.
Чтобы полностью избежать этого эффекта, используйте pH-электрод со встроенным датчиком температуры. В этом случае датчик температуры располагается внутри электрода в непосредственной близости от стеклянной мембраны (Рисунок 3).
Комбинированные pH-электроды с системой сравнения «Long Life»
Большинство pH-электродов на рынке, представляют собой комбинированные pH-электроды с эталонной системой Ag/AgCl. Растворимость хлорида серебра зависит от температуры.
Ионное произведение хлорида серебра в воде очень мало и составляет примерно 10-10 mol2/L2. Однако хлорид серебра очень легко растворяется при комплексообразовании. Этому эффекту способствует повышение температуры, что приводит к изменению равновесия между твердым и растворенным хлоридом серебра. Поэтому при изменении температуры необходимо дождаться, пока снова не будет достигнуто устойчивое равновесие, так как оно определяет потенциал электрода сравнения.
Благодаря системе сравнения «Long Life», используемой в pH-электродах Metrohm (Рисунок 4), термодинамическое равновесие между серебром, хлоридом серебра (твердым) и хлоридом серебра (растворенным) устанавливается очень быстро, и потенциал референскного электрода становится стабильным довольно быстро.
Калибровка pH-электрода
pH-электроды Metrohm разработаны в соответствии со стандартом DIN 19263. Эти электроды показывают потенциал 0 мВ (zero point) около pH 7.
Рассматривая калибровочные кривые (изотермы) рН-электродов при различных температурах в идеальных условиях, можно было бы ожидать их пересечения в zero point электрода. Но в реальности с pH-электродами дело обстоит иначе. Образуется изотермическая точка пересечения (Рисунок 5), близкая к zero point электрода. Насколько близко зависит от состояния самого электрода.
Чтобы свести к минимуму подобные эффекты, калибровку pH-электрода следует проводить при той же температуре, которая будет использоваться для последующих измерений pH.
Температура измеряемых растворов
pH чистой воды при 25 °C составляет 7,00. В этом случае в воде присутствует равное количество ионов гидроксония и гидроксида. Из-за температурной зависимости ионного произведения воды это равновесие смещается в сторону более высокого pH при более низких температурах и наоборот. Эти сдвиги равновесия известны для буферных растворов и известных кислот и оснований (см. примеры в Таблице 2), но не для всех типов растворов образцов.
Таблица 2. Три примера, показывающие, как изменения температуры могут повлиять на значение pH образца [3].
| рН растворов, измеренный при разных температурах | 0 °C | 25 °C | 50 °C |
|---|---|---|---|
| H2O | 7.47 | 7.00 | 6.63 |
| c = 0.001 mol/L HCl * | 3.00 | 3.00 | 3.00 |
| c = 0.001 mol/L NaOH | 11.94 | 11.00 | 10.26 |
* Температурные эффекты слабее при определении рН кислых веществ. В этих случаях наблюдается общая тенденция к увеличению значения рН с повышением температуры.
Даже самые современные рН-метры могут корректировать температурное поведение только электрода, но не измеряемых растворов. Для правильных измерений pH очень важно всегда измерять значение pH ваших образцов при той температуре, при которой они были отобраны. Например, если образец отбирается при температуре 10 °C, то калибровку pH-электрода и измерение образца также следует проводить при 10 °C. Следование этому правилу помогает избежать нежелательных эффектов температурного равновесия и приводит к быстрому отклику pH-электрода.
Заключение
Благодаря оптимизированной конструкции реальное поведение высококачественных pH-электродов Metrohm лишь незначительно (максимальная асимметрия потенциалов +/- 15 мВ) отличается от идеальных значений. Однако, как и в большинстве случаев, здесь задействовано более одного фактора.
Приведенный ниже чек-лист поможет вам получить точные результаты измерений во время калибровки и измерения pH. Если вы можете ответить ДА на все перечисленные пункты, вы учитываете большинство эффектов, вызванных изменениями температуры.
| ДА / НЕТ | |
|---|---|
| ( ) | Я выбрал(а) правильный стеклянный pH-электрод, учитывая тип мембранного стекла для моей задачи. |
| ( ) | Мой комбинированный pH стеклянный электрод оснащен референсной системой «Long Life». |
| ( ) | Температурный датчик расположен близко к стеклянной мембране рН-электрода. ИЛИ Я использую комбинированный стеклянный pH-электрод со встроенным датчиком температуры для калибровки/измерения pH. |
| ( ) | Мой рН-метр имеет встроенную температурную коррекцию. |
| ( ) | Калибровка проводится при той же температуре, что и все последующие измерения pH. |
| ( ) | Все измеряемые образцы имеют одинаковую температуру. |
References
[1] Degner, R.; Leibl, S. PH Messen: So Wird’s Gemacht!; Wiley, 1995.
[2] Galster, H. PH-Messung: Grundlagen, Methoden, Anwendungen, Geräte; VCH, 1990.
[3] pH und Temperatur – zwei untrennbare Größen. Wiley Analytical Science. https://analyticalscience.wiley.com/do/10.1002/was.00050234 (accessed 2023-02-09).
Your knowledge take-aways
Monograph: pH measurement Everything from A – Z
Flyer: Electrodes for pH measurements - Which electrode for which application?
Application Bulletin: pH measurement technique
Blog: How to calibrate a pH meter
 Поделиться статьей
Поделиться статьей

 Поделиться статьей
Поделиться статьей